Info-Tech Live 2026
Join Modern Requirements at Info-Tech Live 2026 and witness firsthand...

Le développement de logiciels médicaux désigne le processus par lequel les entreprises développent des applications destinées tant aux patients qu'aux professionnels de santé. Une gestion rigoureuse des exigences constitue un élément essentiel de la réussite dans le développement de logiciels pour dispositifs médicaux. Ces outils aident les équipes à concilier les besoins des utilisateurs, les impératifs commerciaux et les réglementations strictes. À mesure que la concurrence s'intensifie dans ce secteur, il devient de plus en plus difficile de trouver un équilibre entre ces différents enjeux. Selon Statista, le marché des dispositifs médicaux devrait atteindre 609 milliards de dollars de chiffre d'affaires d'ici 2028, contre 471 milliards aujourd'hui.
Alors que l'innovation fait progresser le secteur, les exigences en matière de précision, de conformité et d'efficacité ne cessent de croître. Cet article aborde les défis courants du secteur des logiciels médicaux et explique comment les solutions de gestion des exigences peuvent vous aider.
Les entreprises du secteur des dispositifs médicaux sont confrontées à des défis différents et plus importants que les autres entreprises. Les obstacles réglementaires, les enjeux pour les utilisateurs finaux et la complexité de la gestion de projet constituent des freins majeurs. Tout logiciel qui vous aide à surmonter ces défis devient également un outil de gestion des risques dans le domaine de la santé. Voici quelques-uns des défis courants auxquels les entreprises sont confrontées dans le développement de logiciels pour dispositifs médicaux :
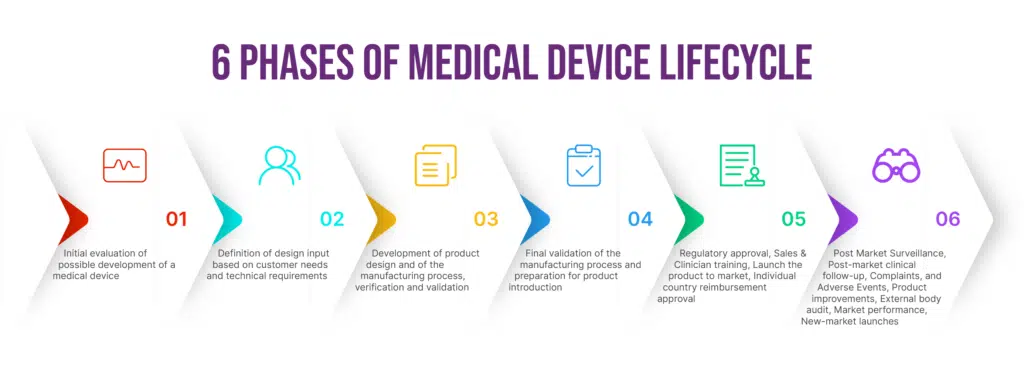
Les logiciels destinés aux dispositifs médicaux constituent un élément essentiel des solutions de santé modernes. Leur développement exige une approche rigoureuse afin de garantir leur fonctionnalité, leur sécurité et leur conformité réglementaire. Les outils de gestion des exigences constituent la base du succès, en offrant un cadre structuré permettant de recenser, d'analyser et d'assurer la traçabilité de tous les aspects des exigences logicielles.
La méthode traditionnelle de gestion des exigences dans le domaine du développement des soins de santé n' est pas adaptée au développement de logiciels pour dispositifs médicaux. Avec cette méthode, les équipes chargées du matériel et celles chargées des logiciels répondaient séparément à ces besoins après s'être mises d'accord sur les besoins des parties prenantes. Cependant, elles utilisaient des outils et des méthodologies différents, ce qui entraînait des problèmes de traçabilité et des retouches coûteuses.
Cela entraîne un long processus de recherche et de résolution des problèmes entre les deux équipes et peut prendre beaucoup de temps qui aurait pu être consacré à l'amélioration de l'appareil.
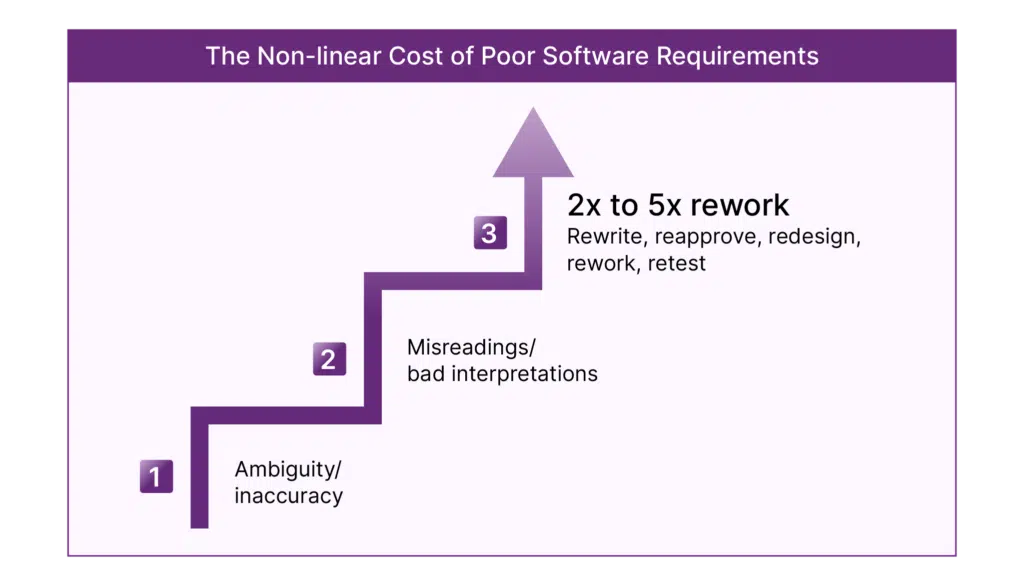
Pour gérer la complexité des produits, les interfaces utilisateur, les réglementations et les données des patients, des outils de gestion des exigences sont indispensables. Ils rationalisent le développement et le déploiement des logiciels et atténuent les risques liés à la conception des dispositifs médicaux et de leurs logiciels. Les meilleures solutions de gestion des exigences s'appuient sur des plateformes existantes largement utilisées, telles qu'Azure DevOps, pour en faire une source unique de vérité. Elles permettent également, par extension, de gérer les risques liés au secteur de la santé.
Dans le secteur de la santé, le respect des exigences réglementaires est essentiel au succès des dispositifs médicaux. On estime que le marché mondial compte au total deux millions de dispositifs médicaux, répartis en environ 7 000 catégories. Ces dispositifs doivent satisfaire aux normes réglementaires internationales, locales et spécifiques à leur catégorie.

Ces normes sont établies par des organismes de réglementation tels que la Food and Drug Administration (FDA) aux États-Unis et l'Agence européenne des médicaments (EMA) en Europe. Rien qu'aux États-Unis, la FDA exige que les dispositifs médicaux répondent à au moins sept exigences réglementaires fondamentales. Ces normes couvrent un large éventail d'aspects liés aux dispositifs médicaux, de la conception à la surveillance post-commercialisation. Un glucomètre standard peut être tenu de respecter la liste suivante (non exhaustive) de normes :
| Fonction | Règlement (le cas échéant) | Norme de conformité | Niveau |
| Prévention des infections | Recommandations du CDC relatives à la prévention des infections lors de la mesure de la glycémie | Certificat de conformité (CoC) ou certificat d'accréditation (CoA) de la CLIA | National (États-Unis) |
| Conception et utilisation de l'appareil | Directives de la FDA relatives aux systèmes d'autocontrôle de la glycémie | ISO 15197 | National (États-Unis) |
| Signatures électroniques | Titre 21 du Code des règlements fédéraux, établi par la FDA. | CFR, partie 11 | National (États-Unis) |
| Gestion des risques | N/A | ISO 149715 | International |
| Processus du cycle de vie des logiciels | N/A | IEC 623046 | International |
| Sécurité des logiciels de santé | N/A | IEC 82304-17 | International |
| Sécurité des appareils électromédicaux | N/A | IEC 60601-18 | International |
Les outils de gestion des exigences jouent un rôle crucial dans la mise en conformité des dispositifs médicaux avec les normes. Une équipe doit documenter, analyser, assurer la traçabilité et hiérarchiser les exigences auxquelles elle doit satisfaire. En gérant efficacement les exigences, les fabricants de dispositifs médicaux peuvent s'assurer que leurs produits non seulement respectent les normes réglementaires, mais offrent également des solutions sûres et efficaces aux professionnels de santé et aux patients.
Dans le domaine médical, où les enjeux sont considérables et où la précision est primordiale, la rigueur est indispensable. Les outils de gestion des exigences permettent aux équipes de développement de définir et de documenter les exigences logicielles avec une grande minutie.
Lors de la création de logiciels destinés aux dispositifs médicaux, les équipes peuvent recourir à plusieurs fonctionnalités offertes par les outils de gestion des exigences, telles que :
Les entretiens avec les parties prenantes constituent un exemple concret de technique de recueil des exigences. Le facteur le plus important dans le recueil des exigences par le biais d'entretiens réside dans les questions que vous posez. Il est préférable de procéder à ce recueil dès les premières étapes de la conception du prototype. Une liste de FAQ préexistante et modifiable peut vous aider à rassembler les bonnes questions pour ce recueil. Un outil d'IA intégré peut également générer des questions spécifiques au projet en analysant les données brutes relatives aux exigences.
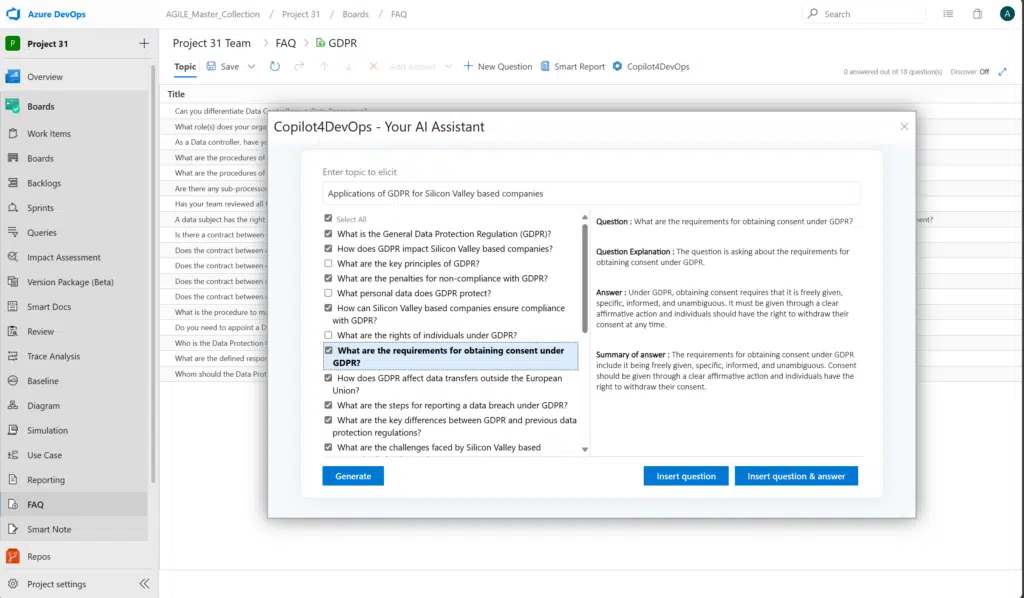
De nombreuses erreurs peuvent se glisser dans la documentation en raison de délais serrés et d'une concurrence acharnée. Plus d'un tiers des ingénieurs en logiciels considèrent qu'une documentation de mauvaise qualité constitue l'un de leurs principaux défis. Cela revêt une importance encore plus cruciale dans le domaine du développement de logiciels pour dispositifs médicaux.
La création aisée de documents de spécifications structurés, de type Word, au sein d'une plateforme ALM telle qu'Azure DevOps peut contribuer à réduire ces erreurs.
La complexité liée à la coordination du développement matériel et logiciel peut être source d'erreurs. Il est facile de perdre de vue les liens entre les différentes tâches. La création de matrices de traçabilité permettant de suivre les exigences de bout en bout peut contribuer à réduire ces erreurs. Cela favorise également l'efficacité du projet, les tests des composants, l'analyse d'impact et la communication au sein de l'équipe.
Dans ce genre de situation, il est très pratique de pouvoir générer en un seul clic des rapports sur tous les aspects de votre projet.
C'est encore mieux si vous pouvez exporter ces documents au format PDF, Word ou HTML.
Modern Requirements4DevOps est une solution conçue pour rationaliser le processus de gestion des exigences dans le développement de logiciels destinés aux dispositifs médicaux. Ses principales fonctionnalités comprennent la traçabilité, la collaboration et la gestion des changements, qui améliorent l'efficacité des projets et garantissent la conformité aux normes réglementaires. Elle intègre également un outil d'IA révolutionnaire appelé Copilot4DevOps, qui améliore la qualité des exigences grâce à la collecte, à l'analyse et à bien d'autres fonctionnalités.
En tirant parti de Modern Requirements4DevOps, des organismes de santé tels que Bayer et la Croix-Rouge garantissent une meilleure conformité réglementaire, une efficacité accrue des projets et une réduction des coûts de développement. Voici comment vous pouvez vous aussi l'utiliser.
Une gestion efficace des exigences est essentielle dans le développement de logiciels pour dispositifs médicaux. Bien que les outils de gestion des exigences constituent le meilleur moyen d'optimiser votre projet, il existe également certaines bonnes pratiques qui s'appliquent quel que soit l'outil utilisé :
À mesure que le marché des dispositifs médicaux se développe, il sera de plus en plus difficile de concilier matériel, logiciels et réglementation. Un outil de gestion des exigences performant est votre allié pour gérer ces complexités.
Grâce aux dernières avancées en matière d'intelligence artificielle, ces outils rationalisent le développement, garantissent la conformité réglementaire et réduisent les risques. Ils s'appliquent aussi bien aux logiciels qu'au matériel des dispositifs médicaux. À mesure que le secteur évolue, ces outils joueront un rôle essentiel dans la réussite des projets, stimuleront l'innovation et contribueront à améliorer les résultats pour les patients.
✅ Définissez, gérez et suivez les exigences dans Azure DevOps
✅ Collaborez en toute fluidité entre équipes soumises à des réglementations
✅ Commencez GRATUITEMENT — aucune carte de crédit requise
Join Modern Requirements at Info-Tech Live 2026 and witness firsthand...
Learn how to automate FedRAMP SSP and POA&M documentation to...
Learn how to trace, maintain, prioritize, and control requirements throughout...
End-to-end requirements management in Azure DevOps.
AI-powered assistance for DevOps workflows.
Autonomous AI agents for DevOps execution.
Real-time data sync across tools and systems.
Designed to work natively within Azure DevOps, Modern Requirements extends the platform with powerful capabilities that help teams capture, manage, and validate requirements more effectively.